การทดสอบเกี่ยวกับการเกิดพิษจากสารตะกั่ว
การเกิดพิษจากสารตะกั่วส่วนมากแล้วมาจากผู้ทำงานในโรงงานที่หลอมตะกั่ว ผู้ที่ทำงานในโรงงานซ่อมแบตเตอรี่ ผู้ที่ทำงานในการตัดท่อนเหล็กด้วย acetylene อาจได้รับสารตะกั่ว ถ้าท่อนเหล็กนั้นถูกทาด้วยสีที่ผสมตะกั่ว
การที่ร่างกายได้รับสารตะกั่วเข้าไปจะมีผลต่อการ synthesis ของ heme นั่นคือ Delta-am inolevulinicacid dehydrase (ALA-D) ซึ่งเป็นตัวเปลี่ยน ALA ไปเป็น porphobilinogen จะมีความเข้มข้นน้อยลงหลังจากที่ได้รับสารตะกั่วเข้าไปในร่างกาย ได้ 4 วัน (ตามรูป 1) เมื่อ ALA-D เริ่มลดลง ก็จะมีปริมาณของตะกั่วอยู่ใน body tissue ดังนั้น ALA-D ก็จะมีปริมาณลดลงตราบใดที่มีตะกั่วอยู่ นั่นคือค่าของ ALA-D จะมีปริมาณน้อยอยู่เป็นปี แม้ว่าผุ้ป่วยจะไม่ได้สัมผัสกับตะกั่วแล้วก็ตาม ดังนั้นปริมาณของ ALA-D ก็จะเป็นสิ่งที่บอกได้ที่ผู้ป่วยนั้นมีการเกิดพิษของตะกั่วหรือไม่ และปริมาณของ ALA-D จะลดลง ประมาณ 50% ของค่าปกติ ถ้ามีตะกั่วอยู่ในเลือด 30-50 ug% แต่เราจะไม่ทราบมากกว่านั้น ถ้าร่างกายของผู้ป่วยได้รับตะกั่วมากกว่า 30-50 ug% เพราะค่าของ ALA-D จะลดลง ถึงขีดจำกัดที่แห่งหนึ่ง และจะไม่ลดอีกต่อไป
รูปที่ 1 การเกิดการลดลงของ ALA-D และการเพิ่มของ ALA
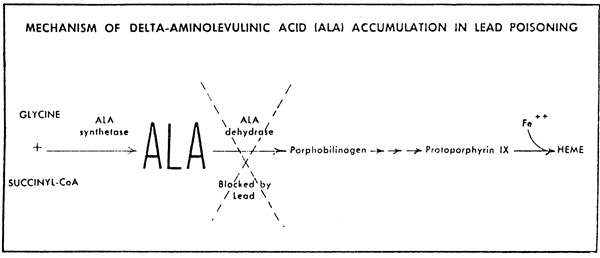
การเพิ่ม ALA ในปัสสาวะ ในกรณีเกิดพิษจากตะกั่วก็เนื่องจาก ALA-D จะถูกทำให้ไม่เกิดปฏิกิริยา เพื่อจะเปลี่ยน ALA ให้ไปเป็น Porphobilinogen ALA จะถูกเก็บสะสมใน body fluid และบางส่วนจะถูกขับออกมาในปัสสาวะ ในกรณีที่เกิดพิษจากสารตะกั่ว ค่าของ ALA จะมากกว่าค่าปกติเกือบ 5 เท่า บางครั้ง ALA อาจจะเพิ่มโดยไม่เพิ่ม CP3 ถ้าผู้ป่วยนั้นเป็น congenital hepatic porphyria
การเกิด CP3 (Coproporphyrinogen III ) เกิดเนื่องจากมีการยับยั้ง ALA-D เช่นกัน ทำให้ CP3 ไม่สามารถเปลี่ยนแปลงไป เป็นสาร protoporphyrinogen IX (รูป 2) ไม่ได้ เป็นผลให้ CP3 ถูกขับออกมาทางปัสสาวะมากขึ้น
รูป 2 การ Synthesis ของ heme และ products ที่เกิดจากสารตะกั่วเป็นพิษในร่างกาย
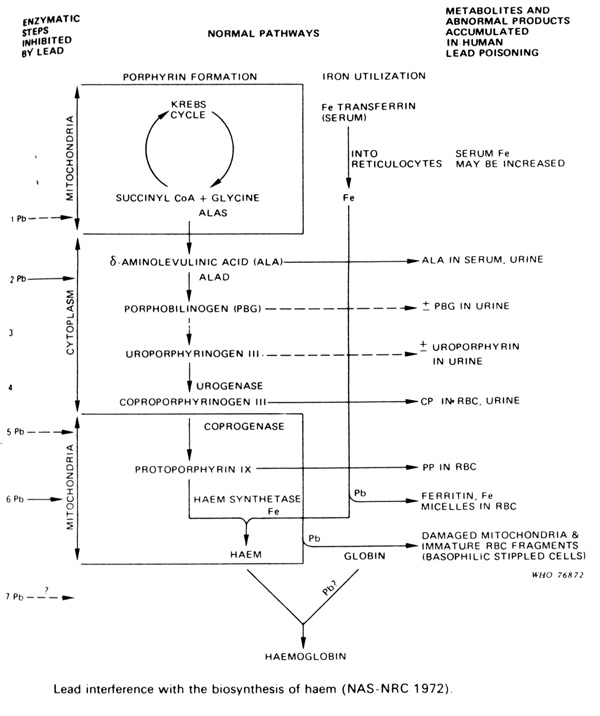
สรุปผลการตรวจทางห้องปฏิบัติการในการตรวจการเกิดพิษจากสารตะกั่ว
1. ค่าซอง ALA-D ในเลือดจะลดลงกว่าค่าปกติ
2. ค่า ALA และ CP3 ในปัสสาวะจะสูงกว่าค่าปกติ
ค่าปกติ
ALA-D = 50-115 units/ml RBC
ALA = 0-6 mg/L
CP3 = 0-200 u/L
ปฏิบัติการที่ 1
การวิเคราะห์ระดับ ALA-D ในเม็ดเลือดแดง
(Determination of ALA-D in RBC)
หลักการ
ทำ hemolyze 0.4 ml เลือดในน้ำ และใส่ buffer substrate ที่มี ALA หลังจาก incubate ในหม้อแช่อุ่นที่ 37°c นำไปตกตะกอนโปรตีนด้วย trichlo¬roacetic acid PBG ที่เกิดขึ้นวัดโดยเติม Ehrlich reagent และวัด activity เป็น units/ml RBC โดยนำค่าของ Hematocrit มาคำนวณด้วย
น้ำยา
1. Substrate
ละลาย 31 มิลลิกรัม ALA-HCl ใน 100 cc. ของน้ำกลั่น และปรับให้ได้ pH = 7 ด้วย saturated NaHCO3
2. Ehrlich reagent
ละลาย 1 กรัมของ p-dimethylamino-benzaldehide ใน 30 ml glacial acetic acid เติม 16 ml ของ 70% HCLO4 ลงไป และเติม glacial acetic acid ให้ครบ 50 ml
3. Trichloroacetic acid 10%
ละลาย 2.7 กรัม HgCl2 และ 10 กรัม TCA ใน 100 ml ของน้ำกลั่น
สิ่งส่งตรวจ
EDTA blood
วิธีทำ
1. เขียนบนหลอดทดลองขนาด 16 X 100 ม.ม. ว่า Blank และ Test
2. ใส่น้ำกลั่น 2.6 ml EDTA blood 0.4 ml และ substrate 2.0 ml ลงโนหลอด Blank และ Test เขย่าผสมให้เข้ากัน
3. จากหลอด Blank ดูดส่วนที่ผสมแล้วมา 2 ml ใส่ในหลอดแก้วก้นแหลม และเติม 10% TCA 2 ml เขย่าผสมกันและวางไว้ในอุณหภูมิห้อง 1 ชั่วโมง
4. จากหลลด “Test” นำส่วนผสมทั้งหมดใส่ในหม้อแช่อุ่น 37 °c นาน 1 ชั่วโมง
5. ดูดส่วนผสมจากหลอด “Test” มา 2 ml ใส่ในหลอดก้นแหลมอันใหม่ที่เขียน “Test” เช่นกัน แล้วเติม 2 ml ของ 10% TCA เขย่าผสม และตั้งทิ้งไว้ในอุณหภูมิห้อง 10 นาที
6. นำหลอดแก้วก้นแหลมที่เขียน Blank และ Test มาปั่นที่ 1,500 r/min ด้วยเครื่อง centrifuge
7. ดูด supernatant ทั้งหลอดที่เขียน Blank และ test มาใส่หลอดแก้วอันใหม่ และเติม Ehrlich reagent ลงไป 2 ml ในหลอด Blank และ test เขย่าผสม และตั้งทิ้งไว้ที่อุณหภูมิห้อง 15 นาที
8. อ่านค่า O.D. ที่ 555 nm.
การคำนวณ
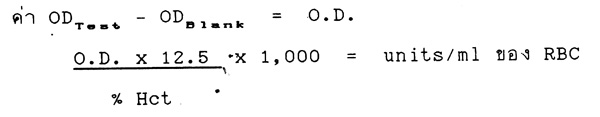
(12.5 = ค่า dilution ของ RBC ในการทำการทดลอง)
ค่าปกติ 50 – 115 units/ml RBC
ปฏิบัติการที่ 2
การวิเคราห์ระดับ ALA ในปัสสาวะ
(Determination of ALA in Urine)
หลักการ
ALA ในปัสสาวะ ทำปฏิกิริยากับ acetylacetone ได้เป็น pyrrole และทำปฏิกิริยาต่อไปกับ p-dimethyl amino benzal dehyde ใน acid solution เกิดสีส้มแดงแล้วนำไปวัดค่าการดูดกลิ่นแสงที่ความยาวคลื่น 553 nm.
น้ำยา
1. Acetylacetone
2. Acetate buffer pH 4.6
ชั่ง sodium acetate 136 กรัมใส่ใน 57 ml ของ glacial acetic acid เขย่าผสมให้เข้ากัน แล้วเติมน้ำกลั่นให้ครบ 1,000 ml
3. Modified Ehrlich’s reagent
ใช้ 50 ml volumetric flask ละลาย 1 กรัมของ p-dimethylamino benzaldehyde ใน 30 ml glacial acetic acid เติม 8 ml ของ 70% perchloric acid แล้วเติมให้ครบ 50 ml ด้วย glacial acetic acid
4. Standard ALA solution 1 mg/ml
ใช้ 50 ml volumetric flask ชั่ง 63.9 mg ของ del ta-ALA. HCl ใส่ลงใน volumetric flask เติมน้ำกลั่นให้ครบ 50 ml เก็บใส่ตู้เย็น และสามารถใช้ได้ภายใน 1 อาทิตย์
สิ่งส่งตรวจ
ปัสสาวะที่ใช้ควรเป็น fresh urine ถ้าปัสสาวะต้องทิ้งไว้ค้างคืน ควรทำให้ปัสสาวะเป็นกรดโดยหยด glacial acetic acid และเก็บใส่ตู้แช่แข็งในที่มืดจนกว่าจะนำมาทดสอบ
วิธีทำ
1. นำปัสสาวะมา 1 ml ใส่ในหลอดทดลอง
2. เติม 0.2 ml acetylacetone
3. เติม 8.8 ml acetate buffer
4. เขย่าผสมให้เข้ากัน และใส่ในน้ำเดือด 10 นาที
5. เอาหลอดออกจากหม้อน้ำเดือดและตั้งทิ้งไว้ให้เย็น
6. ดูดส่วนผสมมา 2 ml ใส่ในหลอดทดลองใหม่
7. เติม 2 ml ของ Ehrlich’s reagent ที่เพิ่งเตรียมใหม่ (freshly prepare) เขย่าผสมให้เข้ากัน ตั้งทิ้งไว้ 15 นาที
8. อ่านค่า OD ที่ 553 nm โดยใช้ blank ยองแต่ละ sample ที่เตรียมไว้
9. การเตรียม blank
ทำแบบเดียวกับการทำปัสสาวะที่ต้องการหาค่า ALA ยกเว้นไม่ต้องทำในข้อ 2 คือ ไม่ต้องเติม acetylacetone
10. นำค่า OD ที่อ่านได้ไปหาค่าความเข้มข้นจาก standard curve
Standard curve
1. เอา stock standard มาทำ dilution ตามตาราง
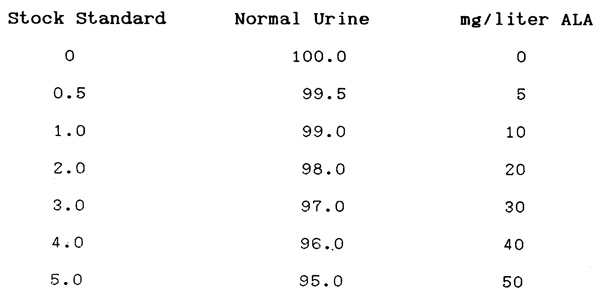
2. เอาจาก working standard มาอย่างละ 1 ml ทำตามวิธีเดียวกับ sample
ค่าปกติ
0 – 6.0 mg/L
ปฏิบัติการที่ 3
การวิเคราะห์ระดับโคโปรพอร์ไพริน III
(Determination of Coproporphyrin III)
หลักการ
CP3 ในปัสสาวะจะถูกสกัดด้วย ether ในภาวะที่เป็นกรด นำชั้นของ ether ซึ่งมี CP3 อยู่มาล้างและสกัดต่อด้วยกรด เมื่อแยก CP3 ออกมาแล้ว วัดค่าการดูดกลิ่นแสงของ CP3 ที่สกัดได้ (ซึ่งจะมีสีชมพูแดง) ที่ความยาวคลื่น 430 และ 401 nm โดยใช้ 0.1 M HCl เป็น blank
น้ำยา
1. Glacial acetic acid
2. Diethyl ether
3. 0.1 M Hydrochloric acid
นำกรด HCl มา 8.55 ml เจือจางด้วยน้ำกลั่นครบ 1000 ml.
สิ่งส่งตรวจ
ปัสสาวะ 24 ชั่วโมง หรือปัสสาวะแบบสุ่มเก็บในขวดสีชา
วิธีทำ
1. เขย่าปัสสาวะให้ผสมกันดี แล้วนำปัสสาวะมา 10 ml ใส่ใน separating funnel
2. เติมกรด glacial acetic acid 0.2 ml แล้วเขย่าผสมให้เข้ากันดี
3. เติม ether 15 ml แล้วเขย่าประมาณ 3 นาที
4. แยกเอาส่วนข้างล่างทิ้ง (เก็บชั้นของ ether ไว้)
5. ล้างชั้นของ ether ด้วยน้ำกลั่นครั้งละ 1 ml 3 ครั้ง
6. ปล่อยน้ำที่ล้างออกทิ้งทุกครั้งที่เติมน้ำ
7. เติมกรด 0.1 M HCl 5 ml เขย่าเมื่อแยก CP จากชั้นของ ether มาอยู่ในชั้นกรด
8. นำสารละลายชั้นกรดออกมาใส่หลอด เพื่อนำไปวัดค่า O.D.
9. นำหลอด unknown ที่สกัด CP3 ได้ไปวัดการดูดกลิ่นแสงที่ความยาวคลื่น 401 และ 403 nm.
การคำนวณ
กรณีที่สกัดด้วย 0.1 M HCl 5 ml
ความเข้มข้นของ CP3 ในปัสสาวะ (Ug/ml) = E401 – E430 X 2
3.58
ค่าปกติ
ค่าปกติของ CP3 ในปัสสาวะ 24 ชั่วโมง = 0 – 200 Ug/L
หมายเหตุ
1. ปัสสาวะที่จะทำการทดสอบ CP3 ควรเก็บใส่ขวดสีชาและรีบทำการทดสอบทันที ถ้ายังทดสอบไม่ได้ในวันนั้น ให้เก็บเข้าตู้เย็นที่อุณหภูมิ 4-8°C และไม่ควรให้ถูกแสง การเก็บในตู้เย็นจะต้องป้องกันแสงได้
2. คาดวัด specific gravity ของปัสสาวะด้วย ปัสสาวะที่ใช้ในการตรวจ ควรมี sp.gr. มากกว่า 1.010 ถ้ามี sp.gr. ตํ่ากว่าค่านี้ ควรจะเก็บปัสสาวะใหม่
การตรวจหายาฆ่าแมลงชนิดออร์กาโนฟอสเฟต
ปฏิบัติการที่ 4
การวิเคราะห์ระดับโฆลีนเอสเตอเรส
(Cholinesterase = ch E.)
หลักการ
เอนไซม์โฆลีนเอสเตอเรส จะกระตุ้นให้มีการแตกตัวของ cholinesters จากกรด organic ชนิดต่างๆ ซึ่งรวมทั้ง acetylcholine ซึ่งใช้เป็น substrate ในการทดสอบโดยมี indicator ที่มี pH เป็นกรด-ด่าง ได้แก่ M-nitrophenol ตาม ปฏิกิริยาดังต่อไปนี้

acetic acid ที่ได้จะทำให้ค่าของ pH ตํ่าลงมาอยู่ในภาวะเป็นกรด ซึ่งจะทำให้สีเหลืองของ M-Nitrophenol จางลง สีที่เกิดขึ้นนี้จะมีค่าเป็นสัดส่วนตรงกับค่าของเอนไซม์โฆลีนเอสเตอเรส
น้ำยา
1. Sodium chloride solution 0.15 mol/L
ใส่ chloroform ลงในน้ำยาที่เตรียมแล้ว 2 มิลลิลิตร เพื่อเป็นสารกันเชื้อรา (preservative)
2. M – Nitrophenol solution

นำสารเบอร์ 1 และเบอร์ 2 มาผสมกัน แล้วปรับ pH ของสารละลายให้ เป็น pH = 7.8 ด้วย 0.1 N NaOH หรือ 0.1 M HCl เติมน้ำกลั่นให้ควบ 500 มิลลิลิตร
3. Acetylcholine chloride solution
Acetylcholine chloride 750 มิลลิกรัม
น้ำกลั่น 5 มิลลิลิตร
เขย่าผสมกัน และเก็บในตู้เย็น ( 2-6°C) จะ stable ได้ 2 อาทิตย์
4. Acetic acid solution 0.02 N.
เตรียมแล้วเก็บไว้ที่อุณหภูมิห้อง (18-26°C) และปิดจุกให้แน่น
สิ่งส่งตรวจ
1. ซีรั่ม
2. พลาสมาที่ใช้ heparin เป็น anticoagulant
วิธีทำ
1. เขียนบนหลอดทดลองขนาด 16 X 100 ว่า Test และ Blank
2. ไปเปตต์ 0.2 ml Sodium chloride solution และ 0.2 ml ลงไปทุกหลอด
3. นำหลอดที่เขียนว่า Blank ไปแช่ในหม้อแช่อุ่น (water bath) 60°c นาน 10 นาที เมื่อครบแล้วนำมาตั้งทิ้งไว้ให้เย็น ส่วนหลอดที่ label Test ให้ตั้งไว้ที่อุณหภูมิห้อง 25°c
4. ทั้ง Blank และ Test เติม 3.0 ml H2O, 2.0 ml M-Nitrophenol solution และ 0.2 ml Acetylcholine chloride solution เขย่าผสมกัน และตั้งทิ้งไว้ที่อุณหภูมิห้อง 25°c
5. ครบ 30 นาที เทสารละลายลงใน cuvet แล้วอ่านค่าการดูดกลิ่นแสงที่ความยาวคลื่น 440 nm โดยใช้น้ำเป็น Blank
การคำนวณ
![]()
นำค่า sA ไปอ่านจาก calibration curve
Calibration curve
1. นำ Test tube 16 X 100 ม.ม. เติม 2.0 ml sodium chloride solution และ 2.0 ml pooled serum เขย่าผสมกัน นำไปแช่ในหม้อแช่อุ่น 60°c 10 นาที เมื่อครบเวลาแล้วนำหลอดมาตั้งทิ้งไว้ให้เย็น ซีรั่มที่ได้นี้เรียก inactivated serum
2. เตรียมหลอดแก้ว 16 X 100 ม.ม. มา 7 หลอด แล้วทำตามตารางข้างล่าง
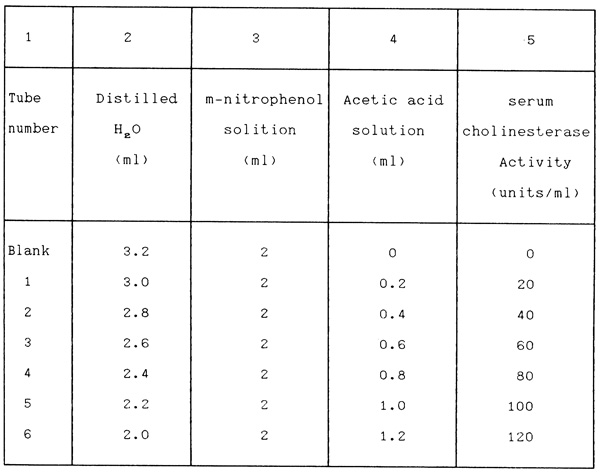
3. อ่าน OD ที่ 440 nm โดยใช้ H2O set zero
4. ลบค่า absorbance ของทุกตัวที่อ่านได้กับค่าของ Blank
![]()
5. ฟล๊อตค่า sA กับ units/ml ของ serum cholinesterase
หมายเหตุ
1. ถ้าค่าที่ได้มากกว่า 100 units/ml ให้ dilute ด้วย sodium chloride solution โดยใช้ปริมาตรเท่าๆ กัน
2. เนื่องจากไม่มีเครื่องมือที่จะหยุดปฏิกิริยา ฉะนั้นให้อ่านค่าการดูดคลื่นแสงทันทีที่ครบ 30 นาที ถ้าอ่านมากกว่า 30 นาที จะทำให้เกิด false positive
Normal Value
40-120 units/ml ถ้าถูกสาร organophosphate ค่าที่ได้จะต่ำกว่า 40 units/ml.
ปฏิบัติการที่ 5
โฆลีนเอสเตอเรสในเม็ดเลือดแดง
(RBC acetylcholinesterase – pH metric method)
หลักการ
เป็นการหาค่า activity ของโฆลีนเอสเตอเรสจากความแตกต่างของค่า pH ที่วัดได้จากเครื่อง pH meter
น้ำยา
1. Titrate น้ำกลั่นให้ได้ pH 8-8.2
ไปเปตต์ 100 ml ของน้ำกลั่นใส่ในบีเกอร 400 ml เติม 1-2 หยด ของ 0.2% phenophthalein ใน 70% ethyl alcohol, เติม 2-3 หยด ของ 0.1 N NaOH และปรับ pH ของน้ำกลั่นให้ได้ 8-8.2 โดยการเติม NaOH
2. Phenophthalein 0.2%
ละลาย 0.2 กรัม ของ phenophthalein ใน 96% ethyl alcohol และเติมน้ำกลั่นลงไป 27 ml.
3. Acetylcholine chloride 1.25%
ละลาย Acetylcholine chloride 0.1 กรัม ในน้ำกลั่น 8.0 ml (ให้เตรียมก่อนใช้ทุกครั้ง)
สิ่งส่งตรวจ
EDTA blood 1 ml
วิธีทำ
1. ใส่ 4.8 ml ของ titrate distilled water pH 8-8.2 ลงในหลอดทดลอง และใส่เลือดลงไป 0.04
2. นำหลอดทดลองแช่ลงในหม้อแช่อุ่น (water bath) 37°c นาน 5-7 นาที
3. นำหลอดทดลองมาเติม 0.2 ml Acetylcholine solution เขย่าผสม แล้วนำไปวัดหาค่า pH ทันที่ จาก pH meter (pH1)
4. นำหลอดทดลองกลับไปแช่ในหม้อแช่อุ่น 37°c อีก 30 นาที แล้วนำไปวัดหาค่า pH ทันทีจาก pH meter (pH2)
การคำนวณ
pH = pH1 – pH2
การแปลผล
ค่าปกติ pH/ 30 min = 1.0 -1.5
ถ้าได้ค่าตํ่ากว่า 1.0 ถือว่าได้สัมผัสกับสาร organophosphate
ที่มา:ผศ.จินตนา โมกขะเวส
คณะแพทยศาสตร์รามาธิบดี